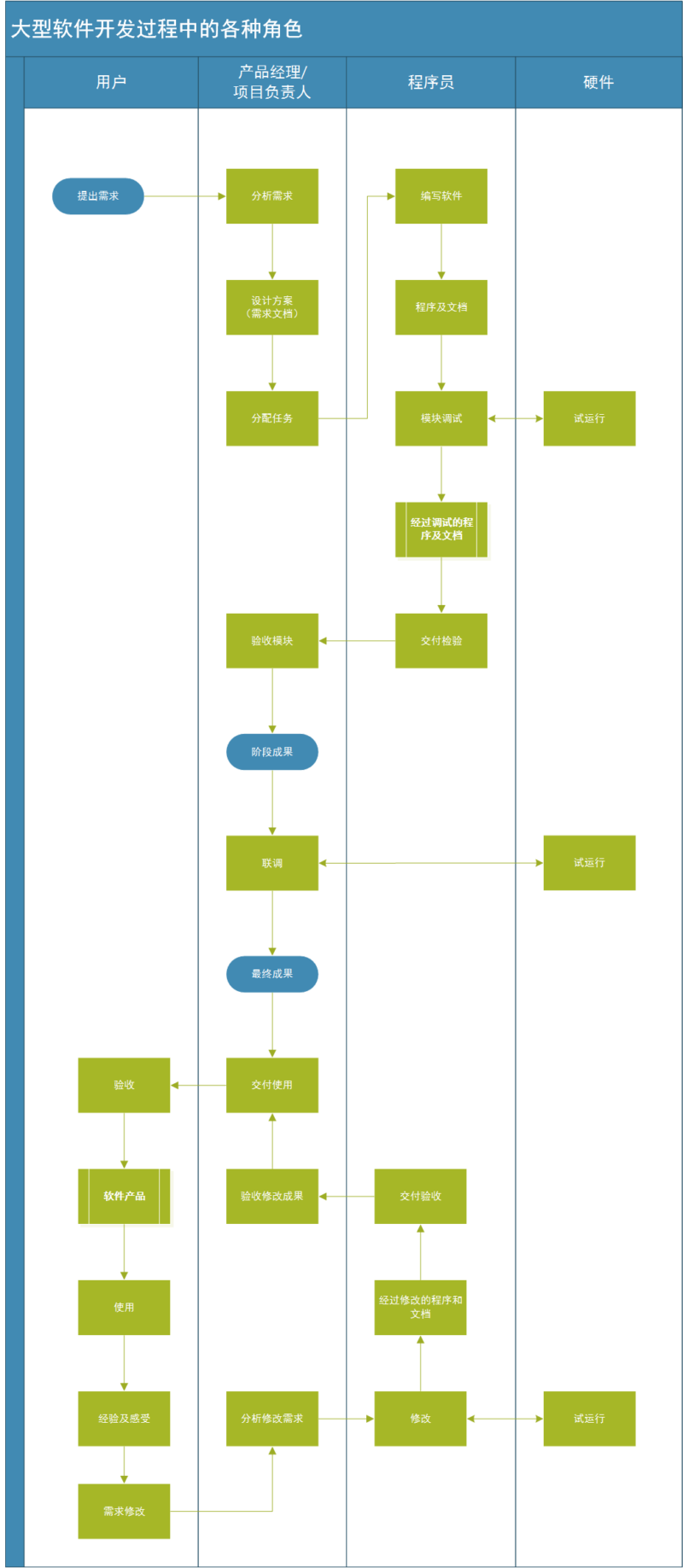
作为医疗器械软件开发者,在将软件产品提交进行测评或注册审批时,准备全面、规范的资料是确保流程顺利的关键。以下是一份详尽的资料清单,并附有开发过程中的关键考量,旨在为开发者提供系统指引。
一、 核心申报与测评资料清单
1. 管理类文件
申请表/覆盖表: 正式的产品测评或注册申请表,明确产品名称、型号规格、版本号等。
符合性声明: 声明产品符合适用的医疗器械法规(如中国的《医疗器械监督管理条例》、欧盟的MDR/IVDR、美国的FDA要求)。
企业资质证明: 开发企业的营业执照、生产许可证(如适用)等。
产品概述与综述资料: 详细描述软件的预期用途、功能、适用人群、临床使用场景、与硬件或其他软件的交互关系等。
* 既往注册/测评历史(如适用): 先前版本的注册证、变更历史、不良事件记录等。
2. 软件技术文档
软件描述文档(核心):
体系结构图: 展示软件模块、组件、内部及外部接口的框图。
- 物理拓扑图(若为网络或分布式系统): 显示硬件部署和网络连接。
- 需求规格说明书(SRS): 包含功能性需求(如算法、用户操作)、性能需求(如响应时间、准确性)、安全需求、网络安全需求、可用性需求等。
- 设计规格说明书(如概要设计、详细设计): 描述如何实现需求。
- 版本历史与变更说明: 完整版本号(通常遵循X.Y.Z构建规则)、各版本变更内容及原因。
- 软件开发过程文档:
- 开发计划、配置管理计划、风险管理计划。
- 验证与确认(V&V)文档: 单元测试、集成测试、系统测试的用例、报告及结果。
- 缺陷管理报告: 发现的缺陷、严重等级、修复状态及验证记录。
- 可追溯性分析报告: 建立从用户需求、到软件需求、设计、代码、测试用例直至风险控制措施的双向可追溯矩阵。
3. 风险管理资料
风险管理计划与报告: 依据ISO 14971标准,系统性地识别、分析、评价、控制和监测软件相关的风险。
风险分析文件: 包括已知和可预见的危害、危害处境、风险估计、风险控制措施及剩余风险评价。
* 风险控制措施验证报告: 证明所实施的安全措施(如报警、权限控制、数据校验)有效。
4. 网络安全与数据安全资料
网络安全描述文档: 说明软件的网络环境、潜在威胁、安全特性(如认证、加密、审计日志)、安全补丁更新机制。
漏洞管理计划: 规定在软件发布后如何识别、评估、修复和披露安全漏洞。
* 数据安全与隐私保护措施说明: 特别是涉及患者健康数据(PHI)的处理、存储和传输时,需符合GDPR、HIPAA或当地相关法规。
5. 可用性/人因工程资料
可用性工程文档: 依据IEC 62366-1标准,描述用户界面设计、使用错误分析和规避措施。
形成性可用性测试报告: 开发过程中进行的用户测试与迭代改进记录。
* 性可用性测试报告: 最终验证产品在模拟使用环境下,用户能安全有效地完成关键任务。
6. 临床评价资料(若软件具有临床功能)
临床评价计划与报告: 证明软件在预期使用场景下的安全性和有效性。可能包括与现有标准方法的对比研究、临床文献回顾、或前瞻性临床试验数据。
算法性能验证报告: 对于采用人工智能/机器学习(AI/ML)或复杂算法的软件,需提供基于独立测试数据集的性能指标(如敏感性、特异性、准确性)验证结果。
7. 标签与说明书
软件用户手册/使用说明: 清晰、完整的操作指南,包含安装、配置、操作、维护、警告和注意事项。
产品标签: 显示软件名称、版本号、制造商、预期用途等信息的屏幕截图或包装信息。
* 发布说明: 提供给用户的本次版本更新内容、已知问题及使用建议。
8. 质量体系相关证明
表明开发过程符合ISO 13485医疗器械质量管理体系标准的声明或证书。
内部审核和管理评审记录(通常在监管机构现场核查时提供)。
二、 给软件开发者的关键建议
- “质量源于设计”(QbD): 从项目启动伊始,就将法规符合性、风险管理、网络安全和可用性要求融入开发生命周期(如采用V模型、敏捷与合规结合的模式),而非在开发后期补充。
- 文档与开发同步: 技术文档应是开发活动的自然产出,确保其真实、及时、可追溯。使用需求管理、测试管理等工具可以提高效率和一致性。
- 重视版本控制: 严格执行软件版本控制(如使用Git),确保任何构建版本都能准确追溯其对应的源代码、需求和测试状态。
- 关注新兴技术法规: 对于AI医疗软件、云服务(SaaS)、移动医疗App等,需密切关注NMPA、FDA、欧盟等监管机构发布的具体指导原则。
- 内部预审与合规检查: 在正式提交前,进行全面的内部审核或聘请第三方顾问进行合规性差距分析,以提前发现问题。
准备这些资料是一个系统性工程,反映了软件作为医疗器械的安全性和有效性受控开发的整个过程。充分、严谨的资料准备不仅能加速测评审批流程,更是产品高质量和开发者专业能力的体现。